Université Dr Moulay Tahar Saida
Master 1 Microbiologie Appliquée
Département de Sciences de la Nature et de la Vie Dr Belgacem Habiba
TP 8 : Séparation des constituants cellulaires par
La technique
de Centrifugation
La centrifugation est une technique de séparation qui permet de récupérer un précipité (culot) et un surnageant. L’appareil qui fait la centrifugation s’appelle centrifugeuse. Elle permet de séparer des constituants de taille et de masse très variables contenus dans un liquide. Ces techniques consistent à séparer les constituants d’une cellule ou d’un organite et comportent deux étapes principales :
a. L’homogénéisation (ou broyage), qui implique la destruction de la membrane plasmique et donne un homogénat.
b. La séparation des organites par des centrifugations.
Objectif :
La séparation des différents constituants cellulaires (membrane, plasmique, REG, noyau…etc…) par fractionnement cellulaire puis par centrifugation en fonction de leur taille, leur densité et leur forme.
Principe de la technique :
1. Fractionnement des cellules :
- Il s’agit de faire éclater les cellules à étudier afin que celles-ci libèrent dans le milieu leurs différents organites, leur noyau, leur membrane plasmique et leur cytosol.
- Plusieurs méthodes peuvent être utilisées : on distingue ainsi les méthodes physiques (ex: rupture mécanique de la membrane plasmique à l’aide d’un piston broyeur) et les méthodes chimiques (ex : dissolution de la membrane plasmique à l’aide d’un détergent). Dans le cas de cellules végétales, il faut auparavant dissoudre la paroi squelettique par le biais d’enzymes adéquates.
- On obtient finalement un homogénat cellulaire.
Matériel :
Centrifugeuse + tubes à centrifuger, balance de précision + spatule + capsule de pesée, 4 béchers de 100 ml, agitateur magnétique + barreau aimanté, 2 mortiers et pilons, 2 entonnoirs + micropipettes (1 ml), 3 béchers de 50 ml ; agitateur de tubes (vortex).
Produits chimiques utilisés : Saccharose et Eau distillée
Echantillons : 3 échantillons utilisées (lycopènes de tomate, carotènes de la carotte et chloroplastes des feuillets de laitue).
Méthodes :
Préparation des échantillons
On découpe les échantillons (feuillet de laitue, carotte et tomate) chacun dans un mortier en broyant à sec, puis on ajoute quelques millilitres de saccharose 3% (dilué) pour permettre l’éclatement des cellules et donc la libération des organites dont les plastes (extraction par osmose), puis on fait une double filtration, pour obtenir des solutions dépourvues de débris cellulaires.
2 . Séparation d’organites cellulaires par centrifugation (centrifugation différentielle) :
La séparation des différents constituants s’effectue par centrifugation différentielle. Le principe consiste à utiliser un champ centrifuge pour séparer les constituants : en effet, la force centrifuge affectant une structure cellulaire, donc la vitesse de sédimentation de celle-ci est d’autant plus forte que sa taille et sa densité sont élevées (la forme de la structure influence aussi la vitesse).
Pratiquement, l’homogénat est placé dans un tube de centrifugation, lui-même placé dans une centrifugeuse. Les noyaux étant généralement les structures les plus grosses de l’homogénat, ils sédimentent les premiers au fond du tube en formant un culot. On arrête alors la centrifugation et on recueille le surnageant. Le culot contenant les noyaux est laissé de côté alors que l’homogénat est placé dans un autre tube et centrifugé à nouveau, à une vitesse plus élevée. Cette seconde centrifugation entraîne la sédimentation des structures intactes les plus grosses en dehors des noyaux (mitochondries en général) qui forment à leur tour un culot. Le processus est répété plusieurs fois, en augmentant progressivement la force centrifuge afin d’obtenir les structures de plus en plus petites.


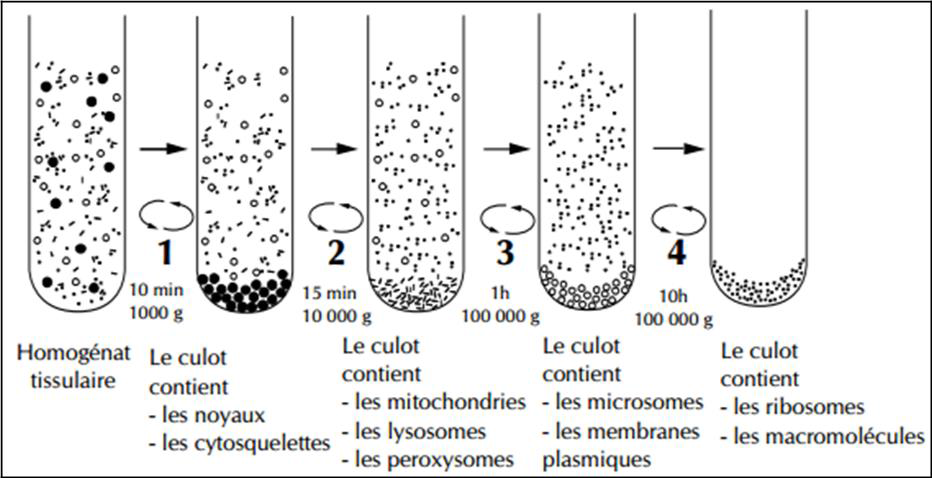
La Centrifugation différentielle
3. Séparation fine des constituants structuraux d’une fraction précédemment obtenue par centrifugation différentielle :
Exemple: on cherche à séparer les mitochondries des lysosomes et des peroxysomes de la fraction 2 de la page d’avant.
La séparation fine des constituants d’une même fraction s’effectue alors par centrifugation en gradient de densité.
Le principe est différent: on réalise dans un tube un gradient artificiel de densité (souvent: un gradient artificiel de saccharose).
Les constituants à séparer sont alors déposés dans ce tube, et ce dernier est centrifugé. Les différents constituants se déplacent alors dans le tube selon leur densité et s’arrêtent quand ils atteignent la zone du tube qui correspond à leur densité.
A noter que cette séparation de constituants par centrifugation en gradient de densité permet aussi la séparation de molécules (ex : ADN, ARN…).
3.1 Préparation des solutions de saccharose 70%, 30%, 5% et 3%
Pour préparer une solution de saccharose 70% ; on pèse, à l’aide d’une balance de précision tarée, 70 g de saccharose (sucre alimentaire). Par la suite, on remplit la fiole de 100 ml contenant ce saccharose par l’eau distillée jusqu’au trait de jauge. Enfin, on fait dissoudre le saccharose dans un bécher de 100 ml, à l’aide d’un agitateur magnétique. On procède de la même manière avec les autres concentrations (30g de saccharose pour la solution de 30 %, 5g pour 5% et 3g pour 3%).
Le gradient discontinu est formé par des dépôts successifs de solution de saccharose de densité décroissante. Dans un tube, mettre 1 ml de saccharose 70% verticalement, ensuite 1 ml de saccharose 30%, position de tube oblique. Enfin, 1 ml de saccharose 5% en position de tube oblique.
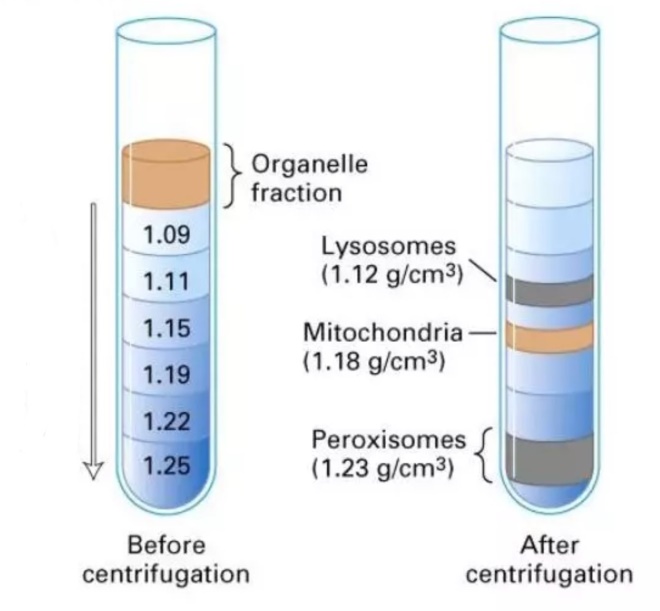
Les différents organites sont obtenus en perçant le tube à la base et en les recueillant ensuite dans des tubes séparément
